こんにちは。なーとし(@naaaaaaato2018)です。
さて今回は、臨床試験を効率的に進められるマスタープロトコルついて、説明していきたいと思います。

なんでマスタープロトコルって必要なの?

開発中の薬剤がどんどん複雑になって、これまで通りのやり方だと時間もお金もかかってしまうからです!
まずは、これまでの臨床試験について振り返ってみます。
これまでの臨床試験を解説
臨床試験とは、『世界中で販売する前に、新規化合物or医療機器orアプリの有効性・安全性を確認するために行う試験』です。
つまり大雑把に言うと、『開発中の製品が有効性・安全性に問題がない』という仮説を立てて、実際にその仮説を検証することになります。
ただし、一度に有効性も安全性も検証するのが難しいので、治験として第Ⅰ相~第Ⅲ相試験を行い、さらに製造販売後臨床試験として第Ⅳ相試験を行うわけです。
次はどのような手続きが必要かを簡単に解説しますね。
臨床試験の流れ
臨床試験の大きな流れは以下のようになります。
治験相談 |
かなり様々な手続きを省いていますが、大雑把にはこの流れになります。
みなさんがイメージする臨床試験は「症例登録の開始~症例対応の終了」だと思いますが、そこに至るまでに、非常に多くの手続きが必要になるのです。
この流れを見れば、

臨床試験ってめっちゃ時間かかるじゃん!!
と思ってもらえると思います。

そうなんです!
臨床試験始めるまでも、めっちゃ時間かかるんだから!!(心の叫び)
これだけ手続きが煩雑なので、「【臨床開発職志望者向け】CRA職を目指す際に求められる能力5選」でも、スケジュール管理能力を挙げています。
最近の薬剤開発状況から見る、臨床試験の問題点
さて、これまでの臨床試験にも問題は多くあります。
問題点の1つとして、薬剤の複雑化に伴い、これまでのプロトコルでは効率が悪くなっています。
これまでの臨床試験は、『1つの疾患に対して、1つの新規化合物の有効性・安全性を確認する』試験でした。
これまでの糖尿病や高血圧のような疾患に対しては、そのアプローチでも問題ありませんでした。
しかし、現在開発中の薬剤との相性が悪くなってきています。
例えば、抗がん剤を筆頭に「Precision Medicine」が注目されています。
Precision Medicineを体現するには、より細かい選択除外基準(試験に参加できる患者さんの条件)が必要になるので、時間もコストもかかるんです。
| 例えば、大腸がん患者を対象とした治験と言っても、開発中の薬剤によっては選択除外基準に「P53の変異を有していること」と規定されることもあります。 すると、「大腸がん患者500人のうち、P53変異を有する人が〇%いて・・・」のように、母数が減っていきます。 |
時間もコストもかかるのに、『1つの疾患に対して、1つの新規化合物の有効性・安全性を確認する』ような従来の臨床試験をしてはいけないわけです。
その問題を解決するのが、マスタープロトコルです。
マスタープロトコルの解説
従来の臨床試験プロトコルの問題点をお伝えしたところで、いよいよマスタープロトコルの解説したいと思います。
そもそもマスタープロトコルとは?
従来の臨床試験のプロトコルは、『1つの疾患に対して、1つの新規化合物の有効性・安全性を確認する』試験でした。
一方マスタープロトコルとは、『1つのプロトコルの中で、複数の疾患に対して、複数の新規化合物の有効性・安全性を確認する』デザインを指します。
現時点でも、抗がん剤の臨床試験で使われ始めています。
一言にマスタープロトコルと言っても、デザインによって以下の3種類に分けることができます。
| ・basket型 ・unbrella型 ・platform型 |
これから、1つずつ順に説明していきます
マスタープロトコル分類わけ
マスタープロトコルの分類わけについては、以下の論文を参考にしています。
basket型
basket型は、『複数の疾患や複数の疾患のサブタイプに対して、1つの新規化合物を投与するデザイン』です。
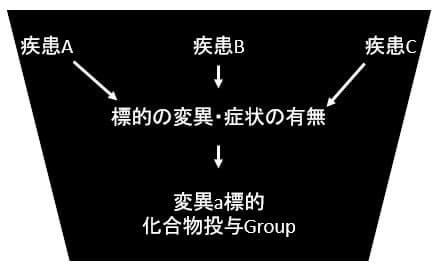
例としては、『P53変異を有する大腸がん、肺がん、肝臓がん患者に対して、P53変異を標的とした新規化合物Aを投与する』試験が挙げられます。
このように遺伝子変異を中心とした開発戦略は今後のスタンダードになることは間違いないと思います。
umbrella型
umbrella型は、『1つの疾患に対して、複数の新規化合物を投与するデザイン』です。

例としては、『大腸がん患者に対して、遺伝子変異の有無に応じて、KRAS変異を標的とした新規化合物A、P53変異を標的とした新規化合物B、PTEN変異を標的とした新規化合物Cのいずれかを投与する』試験が挙げられます。
製薬会社主体でやる際は、パイプラインがかなり豊富でないと難しそうな印象を受けました。
platform型
platform型は、『1つの疾患に対して、複数の新規化合物を半永続的に投与するデザイン』です。
umbrella型との違いが分かりにくいかもしれません。
大きな違いは、事前に決められたアルゴリズムに応じて、「試験に組み込まれる薬剤」や「試験から外される薬剤」が変わってくる点です。
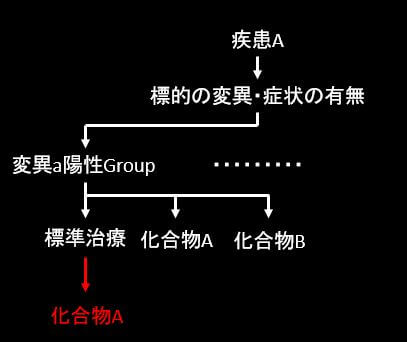
上の図を使って説明すると、白い文字まではumbrella型と大きな違いはありません。
試験から外される薬剤の例を挙げますと、
標準治療と比較して、化合物Aが有効性安全性共に優れていると統計的に判断された時、標準治療が化合物A投与に変わります。(赤字部分)
このように、platform型を活用することで、疾患のサブタイプに応じて、患者さんがベストな治療を受けれる可能性が高まるということです。
また、新たな新規化合物を臨床試験に組み入れることも比較的容易にできます。
他の臨床試験のプロトコルよりも複雑なデザインなので、試験開始時は多少困惑するかもなと思いました。
まとめ
いかがでしょうか?
実は日刊薬業さんでも、マスタープロトコルは取り上げられているんです。

マスタープロトコルを上手く活用することで、煩雑な治験手続きを回避し、同時に複数の試験を進めることができます。
また、「【医薬品開発の立場から考える】2019年以降の製薬業界の動向」や「Virtual Trial (バーチャル治験)とは?~メリットデメリットから事例紹介まで~」の記事でもお伝えしていますが、開発中の薬剤の機序や背景が複雑化していくことに伴い、臨床試験のあり方も変化してきています。
臨床試験に携わるCRAとしては、疾患に対する広範な知識を習得していないと、プロトコルを理解することすらできなくなってしまいます。
ましてや、医師とディスカッションをするのはさらに難しくなるでしょう。
私は今、がん領域を担当していますが、分子生物学の知識があると、本当に楽だなと思いますので、参考になった本を1冊紹介しておきます。
この記事を通じて、マスタープロトコルを活用することで、臨床試験の時間、コストを削減できることが伝われば幸いです。
ではではまた~
合わせて読みたい!!
【月10回出張するビジネスマンが教える】出張時に役立つ荷物&おすすめグッズ5選